贵州省是全国四大中药产区之一,医药产业也是其特 色优势项目,故保证微生物限度检查方法的完整性与可 靠性,是保障当地药品安全的重要组成部分。同名异型中 成药是指名称相同、剂型不同的中成药,贵州省食品药 品检验所近年来相关研究涉及到 7 组该类型,有的是同一 药企产品,有的为不同药企生产。包扩独家品种民族药、 医院制剂,剂型涉及到丸剂、胶囊、片剂、颗粒剂、洗剂、 搽剂。现就上述药品微生物限度检查方法适用性研究过程 及结果进行分析。
1 材料
1. 1 样品
7 组样品共涉及 8 家生产企业,具体如下。 第 1 组: 日 舒 安 湿 巾 ( 批 号 5076001、5076002、 5076003 ) 、 日 舒 安 洗 液 ( 批 号 4066049、 4066080、 4066110) ,贵州汉方药业有限公司。 第 2 组: 妇 科 再 造 胶 囊 ( 批 号 1512003、2026008、 2026012) ,贵州汉方药业有限公司; 妇 科 再 造 丸 ( 批 号 11717053、11717054、11717062) ,贵州德昌祥药业有限公司。 第 3 组: 六味地黄胶囊 ( 批号 20170102、20170103、 20170104) ,贵州圣济堂制药有限公司; 六味地黄丸 ( 批号 DCXA0401、DCXA0421、DCXA0532) ,贵州德昌祥药业有 限公司。 第 4 组: 糖宁通络胶囊 ( 批号 20170601、20170901、 20171001) 、 糖 宁 通 络 片 ( 批 号 20160401、20161201、 20170901) ,贵州百灵企业集团制药股份有限公司。 第 5 组: 复方天麻颗粒 ( 批号 20170914、20170406、 20170710) ,贵州科辉制药有限责任公司; 复方天麻片 ( 批 号 20161003、20170301、20170702) ,贵州百灵企业集团制 药股份有限公司。 第 6 组: 枇 杷 止 咳 颗 粒 ( 批 号 180313、180314、180315) 、枇杷止咳胶囊 ( 批号 180402、180403、180404) , 贵州神奇药业有限公司。 第 7 组: 护 肝 宁 片 ( 批 号 20180104、 20180201、 20180203) ,贵州信邦制药股份有限公司; 护肝宁胶囊 ( 批 号 20160385、20180386、20160387) ,贵州益佰制药股份有 限公司。 其中,第 1、2 组为独家品种,第 4 组为医院制剂。
1. 2 菌种
黑曲霉 [CMCC ( F) 98003]、枯草芽孢杆菌 [CMCC ( B) 63501]、白色念珠菌 [CMCC ( F) 98001]、 金黄色 葡 萄 球 菌 [CMCC ( B) 26003]、铜 绿 假 单 胞 菌 [CMCC ( B) 10104]、生孢梭菌 [CMCC ( B) 64941]、大 肠埃 希 菌 [CMCC ( B) 44102]、乙 型 副 伤 寒 沙 门 菌 [CMCC ( B) 50094],均由中国食品药品检定研究院提供。
1. 3 试剂与培养基
吐温-80 ( 成都金山化学试剂,批号 20170606) 。梭菌增菌培养基 ( 批号 17070161) 、哥伦比亚 琼脂培养基 ( 批号 1707171) 、胰酪大豆胨液体培养基 TSB ( 批号 18030965) 、胰酪大豆胨琼脂培养基 TSA ( 批 号 18042762 ) 、 紫红胆盐葡萄糖琼脂培养基 ( 批 号 17061281) 、溴化十六烷基三甲铵琼脂培养基基础 ( 批号 1512232) 、沙氏葡萄糖琼脂培养基 SDA ( 批号 18010864) 、 沙氏葡萄糖液体培养基 SDB ( 批号 18073161) 、肠道增菌 培养基 ( 批号 1609072) 、甘露醇氯化钠琼脂培养基 ( 批号 1610083) 、麦康凯液体培养基 ( 批号 1703139) 、麦康凯琼 脂培养基 ( 批号 1604055) 、木糖赖氨酸脱氧胆酸琼脂 ( 批 号 17050483) ,均购于北京陆桥技术股份有限公司; RV 沙 门菌增菌液体培养基 ( 批号 3303081) ,购于广东环凯微生 物科技有限公司。
1. 4 仪器
生物安全柜 ( 美国 NuAire 实验设备公司,型 号 NU-425-400E) ; 低温恒温培养箱 ( 型号 KB240) 、电热恒温培养箱 ( 型号 BF240) ( 德国宾德公司) ; 博迅BXM-30R立式压力蒸汽灭菌器[上海博迅提供]; 电子天平 ( 梅特勒-托利多国际有限公司,型 号 ME2002) 。
2 方法与结果
2. 1 供试液制备
按 2015 年版 《中国药典》四部通则 1105要求进行制备。其中,日舒安洗液、咳速停糖浆取 样量为 10 mL,日舒安湿巾取样量为 100 cm2 ,其余品种取 样量为 10 g,分别加 TSB 至 100 mL,制成 1 ∶ 10 供试液, 再据品种实际情况选择合适稀释倍数进行预试验。
2. 2 菌 液 制 备
按 2015 年 版 《中 国 药 典》 四 部 通 则 1105、1106要求进行制备。
2. 3 回收比值计算
计数方法适用性试验中,回收比值 = ( 试验组菌落数-供试品对照组菌落数) /菌液对照组菌落数,添加中和剂组的中和剂回收比值 = ( 中和剂对照组 菌落数-供试品对照组菌落数) /菌液对照组菌落数。2015 年版 《中国药典》 规定,回收比值应在 0. 5 ~ 2 之 间,本实验将其下限提升至 0. 7 左右,以保证该方法在之 后日常检验中重复性更佳。
2. 4 计数方法适用性试验
2. 4. 1 分组
试验组,按要求在供试液加入 “2. 2”项下 菌液,使每 1 mL 供试液中的加菌量不大于 100 cfu,混匀; 供试品对照组,取供试液,以 TSB 代替菌液,其他同试验 组; 菌液对照组,取 TSB 替代供试液,其他同试验组; 中 和剂对照组,取含 1%吐温-80 的 TSB 代替供试液,其他同 试验组。以上 4 组均取 1 mL 混合液,置于 90 mm 培养皿 中,需氧菌总数计数对应组加入 20 mL TSA 培养基,霉菌、 酵母菌计数对应组加入 20 mL SDA 培养基,分别放至 34、 23 ℃培养箱中培养 3、5 d,计数记录。
2. 4. 2 预试验
据药品品种成分及企业反馈信息,分 别在合适稀释倍数下选择各品种对应的敏感菌株进行预试 验,结果见表 1。
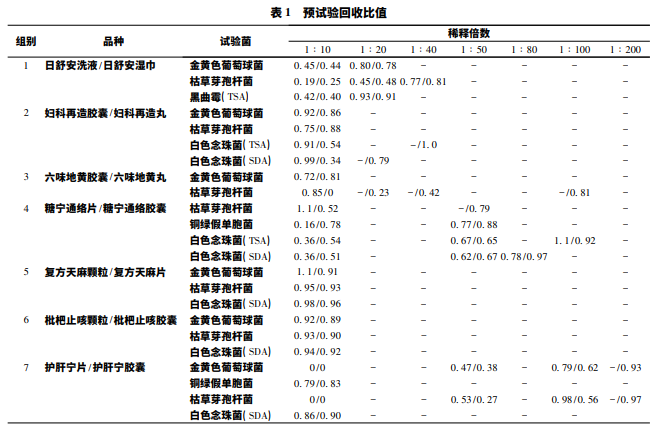
3 讨论
方法适用性试验的本质是建立对样品影响更小、操作 得率更高的方法,但其本身工作量大,而且存在不同实 验室方法欠佳、重复劳动过多的问题,去除药品抑菌性 是其中的重点和难点。因此,本实验在研究前对样品组 分抑菌性进行分析以确定预试验菌株,再根据药典对不同 给药途径的限度规定,确定最终的计数方法; 对控制菌检 查法,主要结合给药途径、是否含药材原粉 2 个方面来开展研究,能有效提高方法适用性试验的效率。